Yenilenebilir Enerji Kaynakları Dersi 7. Ünite Özet
Hidrojen Enerjisi
Giriş
Enerji, insanoğlunun yaşamını sürdürebilmesi için gereksinim duyduğu en önemli olgudur. Bu ihtiyaç günümüze kadar farklı kaynaklar kullanılarak karşılanmıştır. Son yüzyılı dikkate aldığımızda kömür, petrol ve doğal gaz gibi karbonca zengin fosil yakıtlar enerji ihtiyacını karşılamada temel kaynak rolünü üstlenmişlerdir. Fosil yakıtların sınırlı kaynakları olması yanında çevreye verdikleri salımların telafisi güç zararları nedeniyle alternatif enerji kaynaklarına yönlenmenin gerekliliği gün geçtikçe artmaktadır.
Fosil Yakıtlar ve Çevreye Olan Olumsuz Etkileri
İnsanların çeşitli aktiviteleri ve fosil yakıtların enerji elde etmek amacıyla yoğun bir şekilde tüketilmesi sonucu, başta karbondioksit (CO 2 ) olmak üzere halokarbonlar, metan, ozon, azot oksitler gibi gazların ve partikül maddelerin miktarları atmosferde giderek artmakta ve özellikle sebep oldukları sera etkisi nedeniyle küresel ısınmaya neden olmaktadırlar.
Atmosferdeki CO 2 miktarı, 400 bin yıl öncesine ait ve yaklaşık 3625 metre derinlikteki buz kütleleri arasına sıkışmış hava örneklerindeki değer olan 180 ppm’den 400 ppm olan günümüz değerine yükselmiştir. Türkiye’nin atmosfere olan CO 2 salımı 2010 yılında yaklaşık 400 milyon tona ulaşmıştır. Bu yıl itibarıyla Türkiye, CO 2 salınımı açısından dünyayı en çok kirleten ülkeler arasında 20. sırada yer almaktadır.
Küresel ısınma sonucu son 50 yılda Güney kutbunda (Antarktika) 2,5 o C’lik sıcaklık artışı ölçülmüştür. Bunun sonucu olarak Antarktika’da 12 bin yıllık olduğu tahmin edilen Larsen-B adlı 3.250 km 2 ’lik 200 metre derinliğindeki buz dağı ana parçadan ayrılmıştır. Dünyanın en büyük karasal buzullarından İzlanda’daki buzul erimeye başlamıştır.
Kömür, petrol ve doğal gaz gibi fosil yakıtların enerji elde etmek amacıyla yakılarak kullanılması sonucunda oluşan atık gazla atmosfere verilen kükürt dioksit, azot oksitler ve karbon gazları, yağmur damlaları ile birleşerek sırayla sülfürik asit, nitrik asit ve karbonik asit içeren asit yağmurlarını oluşturur. Bu asit yağmurlarının tarım alanlarına, binalara, demir yollarına, köprülere, tarihsel kalıntılara, insanlara ve tüm canlılara zarar verdiği bilinmektedir.
Fosil yakıtların dünyamıza vermekte olduğu zararı öncelikle durdurabilmek ve çok uzun zaman diliminde telafi edebilmek amacı ile en kısa sürede fosil yakıt kullanımı bırakılarak alternatif enerji kaynaklarının kullanımına geçilmelidir.
Birleşmiş Milletler (BM) tahminine göre 2050 yılına kadar dünya nüfusuna 2,5 milyar insanın daha eklenmesi ile nüfusun 9 milyar olması beklenmektedir. Buna karşın günümüz dünyasının temel enerji kaynağı olan fosil yakıtların sınırlı rezervleri olduğu için, bu kaynakların artan nüfus, sanayileşme ve yeni enerji ihtiyaç portföyü ile birlikte gelecek enerji talebine cevap veremeyeceği bir noktaya doğru gidilmektedir.
İdeal bir enerji kaynağı/taşıyıcısı, sınırsız rezervlere sahip olmalı veya kendini yenileyebilmeli, mevcut enerji sistemlerine rahatlıkla entegre olabilmeli, üretim sürecinde fosil yakıtlar mümkün olduğu kadar kullanılmamalı, ihtiyaca rahatlıkla cevap verebilecek şekilde bol üretilebilmeli ve uzun süre özelliğini kaybetmemeli, kullanıcılara her alanda kesintisiz, sürekli aynı kalitede, yeterlikte, kapasitede ve miktarda hizmet verebilmeli, teknolojik gerekliliklere ve uygulamalara yeterince enerji sağlayabilecek güçte ve kapasitede olmalı, kolay ve güvenli olarak üretilebilmeli, enerji kaybı olmaksızın nakledilebilmeli, depolanabilmeli, enerji gerektiren her alanda ihtiyaca yüksek kalitede ve verimlilikte cevap verebilmeli, üretim, nakil, depolama ve tüketim aşamalarında çevre ile uyum içinde olmalı ve olabildiğince çevreye ve ekolojik dengenin varlığına ve sürekliliğine pozitif katkı sağlayabilmeli, birim kütle başına yüksek ısıl değerine sahip olmalı, diğer enerji kaynaklarına verimli bir şekilde dönüşebilmeli, karbon içermemeli ve küresel ısınma, sera etkisi ve iklim değişimi gibi istenmeyen olaylara katkı sağlamamalı ve ekonomik olmalıdır.
Hidrojen ve Özellikleri
Hidrojen kelimesi Yunanca Hydro (su) ve Genes (jeneratör) kelimelerinin birleştirilmesiyle oluşturulmuştur. Günümüzde kabul gören evrenin oluşumu kuramında da belirtildiği gibi, hidrojen bütün yıldızların ve gezegenlerin temel adresidir. Renksiz, kokusuz, tatsız ve zehirli olmayan bir yapıya sahip olan hidrojen, doğadaki en basit atom yapısına sahip olup en hafif ve en yaygın elementtir. Periyodik cetvelin en başında yer alan ve ilk elementi olan hidrojenin atom numarası 1, atom kütlesi 1,00797 olup evrenin kütlesinin %75’ini ve hacminin %90’nını oluşturduğu düşünülmektedir. Su içerisinde hidrojen, oksijen ile bileşik hâlindedir ve suyun %11,2’sini hidrojen oluşturmaktadır. Ayrıca hidrojen insan vücudunun yaklaşık %10’unu teşkil eder.
Kovalent bağ yapma eğiliminden dolayı tabiatta atomik hidrojen (H) neredeyse hiç bulunmaz. Atom olarak hidrojen çok reaktif olup diğer bir hidrojenle birleşerek hidrojen molekülünü (H 2 ) oluşturur.
Hidrojen Enerjisi
Elektrik enerjisi 20. yüzyıla damgasını vuran bir enerji taşıyıcısıdır. Hidrojen ise 21. yüzyıla damgasını vuracak bir diğer enerji taşıyıcısı olmaya adaydır. Hidrojeni cazip kılan avantajlardan bazıları şu şekilde sıralanabilir:
- Kaynak çeşitliliği nedeniyle uygulama esnekliği sağlar.
- Üretimi, taşınması ve depolanması için gerekli teknoloji yeterli olgunluğa erişmiştir.
- Büyük ölçekli altyapı gereksinimi duymadığından, önceden tahmin edilemeyen büyüme veya enerji talep değişimlerine daha hızlı uyum sağlama imkânı sunar.
- Yukarıdaki özelliği sayesinde merkezî sistemlere bağımlılığı azaltır, izole edilmiş küçük topluluklara yerel çözümler ve ekonomik faydalar sunar.
- Temiz bir enerji taşıyıcısı olması nedeniyle çevresel sürdürülebilirliğe katkıda bulunur.
- Boru hatlarıyla emniyetli olarak taşınabildiğinden taşınması sırasında da çevre kirliliğine yol açmaz.
Hidrojenin içten yanmalı motorlarda ve gaz türbinlerinde yakıt olarak kullanılmasını çekici kılan özelliklerinden bazıları, çok fakir karışımlardan çok zengin karışımlara kadar uzanan geniş hava yakıt karışım oranı aralığı içerisinde tutuşabilir olması, yüksek alev hızı ve tutuşma yeteneği, düşük ateşleme enerjisi gerektirmesi, geniş tutuşma ve yanma sınırları, yüksek ısıl değer ve verimdir.
Hidrojenin avantaj ve dezavantaj teşkil eden diğer özellikleri şu şekildedir:
Difüzyon: Hidrojenin diğer gaz yakıtlara göre çok daha yüksek olan hava içinde yayılma katsayısı (0,61 cm 2 /s), emniyet açısından önemli bir sorun oluşturur.
Uçuculuk: Hidrojen, düşük yoğunluğundan dolayı, havada metan, propan veya benzine göre çok daha hızlı bir şekilde yükselir.
Tutuşma için karışım oranı: Hidrojen, metan ve diğer yakıtlara göre çok daha kolay tutuşur.
Tutuşma enerjisi: Hidrojeni tutuşturmak için 0,02 MJ gibi çok düşük enerji yeterli olmaktadır.
Kendiliğinden tutuşma sıcaklığı: Hidrojenin kendi kendine tutuşma sıcaklığı 585 o C’dir.
Vuruntu : Hidrojen kapalı hacimlerde yakılması hâlinde geniş bir konsantrasyon aralığında vuruntu yapar.
Alev hızı: Hidrojenin alev hızı 3,46 m/s olup metanın alev hızı 0,38 m/s ve benzinin alev hızı 0,42 m/s’den çok daha yüksektir.
Alev sıcaklığı: Hidrojenin hava ile stokiyometrik karışımlarında alev sıcaklığı 2207 o C olup metanın alev sıcaklığı olan 1914 o C’den daha yüksek ve benzinin alev sıcaklığı olan 2307 o C’den daha düşüktür.
Hidrojen Üretim Yöntemleri
Hidrojen, birincil enerji kaynaklarından yararlanılarak su, fosil yakıtlar ve biyolojik atıklar gibi değişik hammaddelerden üretilebilen bir enerji taşıyıcısıdır. Günümüzde dünya çapında yıllık hidrojen üretimi 40 milyon ton, 5,6 EJ (1018 Joule) civarındadır. Hidrojen, kömürün gazlaştırılmasıyla da üretilebilmektedir. Hidrojen üretimi için sıralanan yukarıdaki teknikler dışında fotoelektrokimyasal, biyolojik ve biyokimyasal gibi başka teknikler de bulunmaktadır.
Suyun Elektrolizi ile Hidrojen Üretimi
Dünya hidrojen üretiminin %20’sinin karşılandığı bu yöntemle çok saf hidrojen elde edilmektedir. Elektroliz için gerekli olan elektrik enerjisi, fosil yakıtlardan, hidroelektrik kaynaktan, nükleer güçten, jeotermal enerjiden, güneş, rüzgâr ve deniz dalgası gibi yenilenebilir enerji kaynaklarından elde edilebilmektedir.
Elektroliz için gerekli olan elektrik enerjisi, fosil yakıtlardan, hidroelektrik kaynaktan, nükleer güçten, jeotermal enerjiden, güneş, rüzgâr ve deniz dalgası gibi yenilenebilir enerji kaynaklarından elde edilebilmektedir.
Diğer bir elektroliz sistemi ise polimer elektrolit membranın (PEM) ve 2 Amper/cm 2 gibi oldukça yüksek akım değerlerinin kullanıldığı sistemlerdir. PEM elektroliz sistemleri alkali elektrolizörlere göre çok yeni bir teknoloji olup H 2 üretim verimi daha düşük olmasına rağmen özellikle değişken üretimlerin yapıldığı küçük işletmelerde tercih edilmektedir.
Fosil Hammaddelerden Hidrojen Üretimi
Günümüzde sanayide kullanılan hidrojen büyük miktarlarda, doğal gaz, petrol ürünleri veya kömür gibi aynı zamanda birincil enerji kaynağı olarak bilinen fosil yakıtlardan elde edilmektedir. En çok kullanılan yöntemler, doğal gazın katalitik su buharı dönüşümü, petrolün kısmi oksidasyonu ve kömürün gazlaştırılması şeklindedir.
Kömürün Gazlaştırılması ile Hidrojen Üretimi
Kömür dünyanın en zengin fosil yakıtı olup bilinen kömür yataklarına biçilen güvenilir ömür 200 yıl kadar olsa da bunun 400 yıla uzanabileceği söylenmektedir. Hidrojenin kömürün gazlaştırılmasıyla elde edilmesi en eski üretim metodudur ve dünya üzerinde üretilen hidrojenin %18’i bu prosesle elde edilmektedir.
Buhar Dönüşümü (Reforming) ile Hidrojen Üretimi
Hidrojen üretiminde kullanılan en popüler metot katalitik su buharı reforming prosesidir. Prosesin temeli buharla hidrokarbonların nikel katalizör varlığında 750-1000 o C’de reaktörde (reformer) reaksiyona sokularak hidrojen ve karbon oksitlerin elde edilmesidir. Reaksiyon endotermik olduğundan dışarıdan ısı verilmesi gerekir.
Ototermal Reforming (ATR) ile Hidrojen Üretimi
Ototermal reforming yöntemi kısmi oksidasyon ve su buharı reformingi yöntemlerinin birleştirilmiş hâlidir. Kısmi oksidasyon, hidrokarbonların gerekenden az oksijenli ortamda yakılmasıdır. Ototermal terimi, endotermik buhar reformingi ile ekzotermik kısmi oksidasyon reaksiyonları arasındaki ısı alış verişini tanımlar. Ototermal reforming prosesleri, birleştirilmiş tek bir ototermik reaktörde veya gaz ısıtmalı ototermik reaktörler kombinasyonunda yapılabilir.
Isıl (Termal) Ayrışma ile Hidrojen Üretimi
Hidrokarbon bileşikleri oksijensiz ortamda ve çok yüksek sıcaklıklara ısıtıldığında parçalanır, hidrojen ve karbon elde edilir. Bu tip proseslerin en avantajlı tarafı sera gazları emisyonunun olmamasıdır.
Yenilenebilir Enerji Kaynaklarından Hidrojen Üretimi
Yeryüzünün %70’ten fazla kısmı suyla kaplı olduğundan ve suyun %11,2’sini hidrojen oluşturduğundan su, çok bol bulunan bir hidrojen üretim kaynağıdır. Önce sudan hidrojen üretilmekte, sonra üretilen hidrojen havadaki oksijenle birleşerek yandığında tekrar su oluşmaktadır.
Yarı-İletken (Güneş Pili) Sistemler
Güneş pilleri (fotovoltaik hücreler), Güneş enerjisini doğrudan elektrik enerjisine dönüştüren silikon esaslı yarı iletken malzeme içeren sistemlerdir. Güneş pili panelleri birçok fotovoltaik hücreden meydan gelirler. Bu sistemlerde Güneş enerjisi ile hidrojen üretimi iki basamakta gerçekleşir. Burada ilk basamakta, genelde Güneş pili aracılığı ile doğru akım (DC) elde edilir. Daha sonra bu elektrik akımı, bir elektroliz hücresinin elektrotlarına verilerek suyun oksijen ve hidrojene ayrıştırılması gerçekleştirilir.
Fotokimyasal Yöntem ile Hidrojen Üretimi
Bu yöntem, suyu hidrojen ve oksijenlerine ayrıştırmak için, yüksek sıcaklık veya elektriğe gerek olmadan, doğrudan güneş enerjisinin mor ötesi (UV) bölgesini kullanmaktadır. Suyun Termal Parçalanması ile Hidrojen Üretimi Termal güneş gücü fabrikasında merkezî bir kolektörle sağlanan sıcaklık 3000 o C’ye kadar çıkabilmektedir. Oysa su 2000 o C’nin üstünde ısıtıldığında parçalanarak hidrojen ve oksijen’e ayrışmakta, sıcaklık artıkça verim artmaktadır.
Biyokütle Gazlaştırması (Piroliz) ile Hidrojen Üretimi
Ormanlardaki ağaç atıkları, samanlar, yerleşim yerleri katı atıkları, vs. gibi biyokütlenin yüksek sıcaklık ve düşük basınçta gazlaştırılmasıyla da hidrojen elde edilebilir. Biyokütleden hidrojen üretimi fosil yakıtlarından hidrojen üretimine benzer.
Fotobiyolojik Sistemler ile Hidrojen Üretimi
Fotosentetik organizmalar, güneş enerjisini bütün dünyada çok büyük miktarlarda depolayan bir enerji depolama mekanizması oluşturmaktadır. Normal olarak, fotosentetik sistemler CO 2 ’yi karbonhidratlara indirger fakat doğrudan hidrojen vermez. Bugüne kadar H 2 /O 2 üretebilen en verimli fotobiyolojik sistemlerin, yeşil alg ve siyanobakteri gibi algler olduğu anlaşılmıştır.
Hidrojenin Depolanması ve Taşınması
Hidrojen gaz veya sıvı olarak saf hâlde tanklarda depolanabileceği gibi, fiziksel olarak nanotüplerde veya kimyasal olarak hidrür şeklinde depolanabilmektedir.
- Tanklarda Depolama
- Nanotüplerde Depolama
- Metal Hidrürlerde Depolama
- Alanatlarda Depolama
- Bor Esaslı Depolama
Hidrojenin Taşınması
Hidrojen gazı, doğal gaz veya hava gazına benzer olarak borular aracılığıyla her yere kolaylıkla ve güvenli olarak taşınabilmektedir. Doğal gaz için kurulan yeraltı boru dağıtım ağının ileride çok az bir değişiklikle hidrojen içinde kullanılması olanaklıdır. Boru hatları dışında hidrojen, basınçlı tüplerde gaz olarak veya sıvılaştırılmış hâlde tanklara konularak tankerlerle taşınabilir.
Hidrojen Kullanım Alanları
Yakıt hücreleri (pilleri) kimyasal enerjiyi doğrudan elektrik enerjisine çeviren elektrokimyasal cihazlardır. Bunlar yüksek verimlerde çalışmasının yanında sessiz, hafif ve çevre dostudurlar. Günümüzde yakıt hücrelerinin taşınabilir cihazlar, taşıtlar ve güç santrallerindeki uygulamaları yaygınlaşmaktadır.
Genel olarak bir yakıt hücresi güç sistemi, aşağıda verilen dört üniteden oluşmaktadır. Bunlar, yakıt işleme ünitesi, güç üretim sistemi (yakıt hücresi grubu), güç dönüştürücü (inverter) ve kontrol sistemidir.
Yakıt Hücresi Termodinamiği ve Enerji Problemleri
Sabit sıcaklık ve basınçta çalışan bir yakıt hücresinde gerçekleşen elektrokimyasal reaksiyon sonucu elde edilecek maksimum iş (Wel) elektrokimyasal reaksiyonun Gibbs serbest enerjisi değişimi ile aşağıdaki gibi verilmektedir.
Wel = ?G= -nFE
Burada:
n: Reaksiyona katılan elektron sayısı
F: Faraday sabiti (96487 coulomb/g-mol elektron)
E: Hücrenin ideal potansiyeli
?H: Entalpi Değişimi ve ?S: Entropi Değişimi olmak üzere, Gibbs serbest enerjisi ise şu şekilde de ifade edilebilir;
?G= ?H -T ?S
Yakıt ile çalışan cihazlarda termal verimlilik, üretilen kullanılabilir enerji miktarının, ürün ve beslenen akımlar arasındaki entalpi değişimine oranı ile bulunur.

Konvansiyonel motorlarda yakıtın kimyasal enerjisi ilk olarak ısıya daha sonra mekanik enerjiye dönüştürülür. Yakıt hücresinde ise kullanılan yakıttaki kimyasal enerji doğrudan elektrik enerjisine dönüştürülür. Yakıt hücrelerinde ideal bir durumda verimlilik şu şekilde ifade edilir.
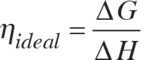
Standart koşullarda (25 o C ve 1 atm) H 2 /O 2 reaksiyonu için ısı enerjisi 285,8 kJ/mol ve iş olarak kullanılabilir serbest enerji 237,1 kj/mol’dür. Bu durumda ideal verim aşağıdaki eşitlikle bulunabilir.
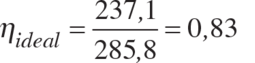
Saf oksijen ve hidrojenle çalışılması durumunda tek hücreli bir yakıt hücresinden termodinamik olarak elde edilebilecek maksimum potansiyel 1,23 Volt dur.
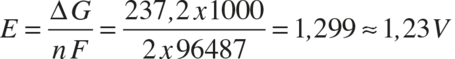
Gerçek sistemlerde bu değer hücre bileşenlerinden gelen etkiler (katalizör deaktivasyonu, membran direnci, yakıt difüzyonu gibi)den dolayı 0,7-1,0 Volt arasındadır.
-
2025-2026 Öğretim Yılı Bahar Dönemi Dönem Sonu (Final) Sınavı Sonuçları Açıklandı!
date_range 6 Gün önce comment 4 visibility 297
-
AÖF 2025-2026 Öğretim Yılı Bahar Dönemi Dönem Sonu Sınavı sorularına itiraz
date_range 12 Mayıs 2026 Salı comment 4 visibility 405
-
2025-2026 Bahar Dönemi Dönem Sonu (Final) Sınavı Sınav Bilgilendirmesi
date_range 4 Mayıs 2026 Pazartesi comment 4 visibility 2318
-
2025-2026 Bahar Dönemi Dönem Sonu (Final) Sınavı Giriş Belgeleri Yayımlandı!
date_range 1 Mayıs 2026 Cuma comment 9 visibility 581
-
AÖF 2025-2026 Öğretim Yılı Bahar Dönemi Ara Sınav sorularına itiraz
date_range 6 Nisan 2026 Pazartesi comment 2 visibility 1852
-
Başarı notu nedir, nasıl hesaplanıyor? Görüntüleme : 27687
-
Bütünleme sınavı neden yapılmamaktadır? Görüntüleme : 16114
-
Harf notlarının anlamları nedir? Görüntüleme : 14409
-
Akademik durum neyi ifade ediyor? Görüntüleme : 13757
-
Akademik yetersizlik uyarısı ne anlama gelmektedir? Görüntüleme : 11617